BİYOLOJİK ARITIMDA AZOT DÖNÜŞÜMLERİ
Atıksudan azot giderimi için kullanılan en yaygın iki metot fiziksel ve biyolojik metottur. Izgaradan geçirme ve çökelme askıda katılara bağlı olan organik azotu giderecek fiziksel yöntemdir. Katı madde giderimleri bazı nutrientleri giderebilirken çözülebilir azotun büyük fraksiyonunu içeren nutrientlerin çoğu giderilemez. Atıksu arıtımında biyolojik azot giderimini doğrudan içeren üç temel biyolojik proses amonifikasyon, nitrifikasyon ve denitrifikasyondur (Whichard, 2001). Biyolojik arıtımda biyolojik azot dönüşümleri Şekil 2.1’de verilmiştir.
Şekil
2.1. Biyolojik arıtmada azotun dönüşümleri
(Metcalf ve Eddy, 2003)
Azot Asimilasyonu:
Heterotrofik ve ototrofik organizmalar NH4+
ve NO3-‘ı alarak assimilasyon (hücre sentezi) için
kullanır. Mikroorganizmalar her ne kadar NO3-‘ı
asimilasyon için kullansa da, nitratı önce amonyuma dönüştürür ve daha sonra
hücre sentezi (protein sentezi) için kullanır. Atıksu
arıtım tesislerinde hücre sentezi için azotun giderilmesi nedeniyle bir miktar
azot giderimi mümkün olur. Bitki ve alg hücreleri azotu amonyum şeklinde tercih
eder. Bu nedenle NH4+ bazlı gübreler NO3-
bazlı gübrelere tercih edilir (Bitton, 1994; URL1).
Azotun bu asimilasyonu çözülebilir
fazdan azotun net bir kaybını meydana getirmesine rağmen giderim sağlayan
azotun temel dönüşümlerinden biri değildir. Azotun giderimini ihtiva eden çoğu
evsel ve yüksek kuvvetli tarımsal atıksularda, bakteriler büyüme için ihtiyaç
duyduğu azotu kullandıktan sonra geriye kalan miktar hala yeterince yüksektir
(Whichard, 2001).
protein → amino asit → amonyum
Amonifikasyon,
organik azotlu bileşiklerin inorganik azota (amonyum, amonyak) dönüşümüdür. Bu
işlem birçok mikroorganizma tarafından gerçekleştirilir (bakteri, aktinomiset,
mantar).Proteinler, aşağıdaki gibi amonyuma dönüştürülürler. Dönüşümden ürease
enzimi sorumludur
Proteinler hücredışı
proteolitik enzimler ile peptit ve amino asitlere dönüştürülür. Amino
asitlerden deaminasyon adımıyla amonyum uretilir. Deaminasyon oksidatif ya da
redüktif olabilir.
NH4+
asidik ve nötral ortamlarda bulunur. Yüksek pH’larda (pH>9) ise amonyum,
amonyağa dönüşür ve amonyak uçucu olup atmosfere karışır (Bitton, 1994; URL 1).
NH4+ → NH3
+ H+
Not: Çevre Mühendisliği Bölümü Lisans Bitirme tezinden bir bölüm. Devamını isteyen arkadaşlar ile paylaşabilirim.

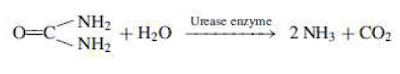

Hiç yorum yok:
Yorum Gönder